 |
| Credit: Cancer Research UK |
Carne roja se refiere a todos los tipos de carne muscular de mamíferos, tales como la carne de res, ternera, cerdo, cordero, caballo o cabra.
Carne procesada se refiere a la carne que se ha transformado a través de la salazón, el curado, la fermentación, el ahumado u otros procesos para mejorar su sabor o su conservación. La mayoría de las carnes procesadas contienen carne de cerdo o de res, pero también pueden contener otras carnes rojas, aves, menudencias o subproductos cárnicos tales como la sangre.
El CIIC ha establecido 5 divisiones:
- Grupo 1- Causa cáncer
- Grupo 2A- Probablemente causa cáncer
- Grupo 2B – Posiblemente causa cáncer
- Grupo 3 – No clasificable como causante de cancer
- Grupo 4 – No causa cáncer
La carne roja se metió dentro del grupo 2A, probablemente carcinógenos para el ser humano. Esto significa en estudios epidemiológicos se ha visto una relación entre el cáncer colono rectal y la ingesta de carne roja, pero que esta evidencia es limitada y que no se pueden descartar que sean otros los factores que hayan afectado esta asociación.
 |
| Credit: Cancer Research UK |
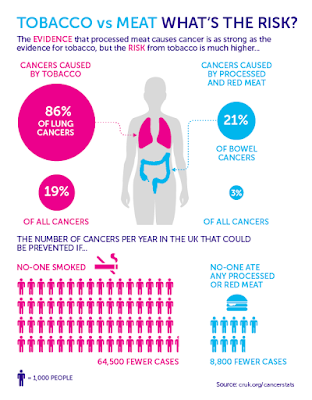
Sin embargo este informe no ha precisado que cantidades podemos consumir de forma segura. Tan solo detallan que un consumo diario de 50g de carne procesada incrementa el riesgo de cáncer colono rectal un 18%.
Quedan aun muchas preguntas por responder como: si no tomo carne procesada a diario, ¿cuanta podría tomar un día concreto sin aumentar mi riesgo de cáncer en un 50%? ¿Y carne roja? Si ya tengo cáncer, ¿debería dejar de comer carne roja? ¿Deberíamos ser todos vegetarianos?
De momento , nos podemos acoger a las recomendaciones dietéticas generals que nos aconsejan no comer mas de 500gr de carne roja a la semana y reducer al máximo el consume de carnes procesadas, como mucho unos 70gr.
También debemos tener en cuenta que no todas las carnes procesadas son iguales y son tantas que la OMS no ha podido hacer recomendaciones individuales. No toda las carnes tienen nitritos y nitratos (cancerígenos), la misma cantidad de sal o conservantes y preservativos.
También debemos tener en cuenta que no todas las carnes procesadas son iguales y son tantas que la OMS no ha podido hacer recomendaciones individuales. No toda las carnes tienen nitritos y nitratos (cancerígenos), la misma cantidad de sal o conservantes y preservativos.
 |
| Credit: Cancer Research UK |
Si quieres saber más sobre como llevar una dieta equilibrada, busca en nuestros servicios el pack de "alimentación equilibrada"
En la foto veréis más o menos cuanta carne hay en una ración de espaguetis o en una sandwich de jamón cocido (fuente Cancer research UK, cuarto link en la lista de abajo).
Si tenéis dudas, escribidnos en los comentarios o consultad estas paginas web para más information:
http://www.nhs.uk/Livewell/Goodfood/Pages/red-meat.aspx
http://www.iarc.fr/en/media-centre/pr/2015/pdfs/pr240_E.pdf
http://www.cancer.org/myacs/newengland/lower-your-cancer-risk-by-eating-right
http://scienceblog.cancerresearchuk.org/2015/10/26/processed-meat-and-cancer-what-you-need-to-know/
Si tenéis dudas, escribidnos en los comentarios o consultad estas paginas web para más information:
http://www.nhs.uk/Livewell/Goodfood/Pages/red-meat.aspx
http://www.iarc.fr/en/media-centre/pr/2015/pdfs/pr240_E.pdf
http://www.cancer.org/myacs/newengland/lower-your-cancer-risk-by-eating-right
http://scienceblog.cancerresearchuk.org/2015/10/26/processed-meat-and-cancer-what-you-need-to-know/



















